
- Casa
- A história de Emily
- Sobre nós
- Investigação
- Eventos
- Imprensa e media
- Tome uma atitude
- Blogue
- Contacto
- Doar

Advocacia
Destacando as necessidades dos últimos 10%
A defesa e representação dos 10% finais da comunidade da FC é uma parte essencial da missão da EE. Embora a EE tenha conquistado uma reputação bem merecida ao longo dos anos pela defesa eficaz da investigação e do desenvolvimento terapêutico para os 10% finais da comunidade da FC, houve uma perceção crescente do seu valor único no espaço regulamentar - e especificamente junto de reguladores importantes como a Food & Drug Administration (FDA).
Em 2021, a EE levou a sua defesa à FDA através de acolher uma sessão de auscultação de doentes da FDA. Este foi um passo importante para a organização. A abordagem da EE à promoção da causa sempre colocou o doente no lugar do condutor, trabalhando lado a lado com a comunidade científica. A parceria com a FDA numa sessão que se centrou especificamente nas necessidades não satisfeitas do 10% final da comunidade da FC reflectiu a voz influente e em expansão da EE em várias áreas fundamentais para o desenvolvimento terapêutico, incluindo o espaço regulamentar.

As sessões de auscultação dos doentes da FDA são pequenas reuniões informais, fechadas ao público, em que os grupos de defesa dos doentes falam com os funcionários da FDA sobre a sua experiência de viver e gerir uma doença. Os objectivos da sessão de auscultação da EE eram partilhar e humanizar as necessidades terapêuticas urgentes e não satisfeitas que subsistem para os 10% finais da comunidade da FC; construir uma relação forte com a FDA para encorajar a definição de prioridades e acelerar as revisões e aprovações regulamentares no futuro; e assegurar que as perspectivas da comunidade da FC são incluídas em todas as fases dos processos de desenvolvimento e aprovação de medicamentos.
Na reunião, a EE informou o pessoal da FDA sobre a EE, a FC e os restantes 10% da comunidade da FC que não beneficiam dos moduladores CFTR atualmente disponíveis, incluindo os portadores de mutações nonsense da FC. O evento incluiu comentários de um clínico e de seis membros da comunidade da FC, incluindo indivíduos com FC, pais e irmãos de indivíduos com FC e um pai de um indivíduo falecido com FC, que partilharam a sua experiência de vida com a doença. Estas histórias profundamente pessoais e sentidas ajudaram a transmitir à FDA a urgência da procura de tratamentos para os restantes 10% da comunidade da FC.
Histórias destacadas nas sessões de auscultação da FDA:
Como parte da sessão de audição da FDA, os participantes ouviram seis membros da comunidade da FC, incluindo Abhijit Tirumala, um estudante universitário de 19 anos com fibrose quística. Como parte do seu testemunho, Abhijit partilhou a forma como a FC afecta a sua saúde mental e como a sua vida mudaria se um novo medicamento pudesse reduzir a sua dependência de tratamentos e medicamentos diários.

Em junho de 2021, a EE realizou sua pesquisa inaugural abrangente e global dos cerca de 10% de indivíduos na comunidade CF que não se beneficiam dos moduladores CFTR atualmente disponíveis devido a mutações inelegíveis, efeitos colaterais ou falta de acesso. O objetivo da pesquisa "Final 10%" foi coletar informações sobre o estado de saúde, o impacto da FC, as necessidades de tratamento não atendidas e as preferências de pesquisa clínica daqueles que não se beneficiam dos moduladores CFTR e apresentar dados e resultados preliminares na Sessão de Escuta da FDA.
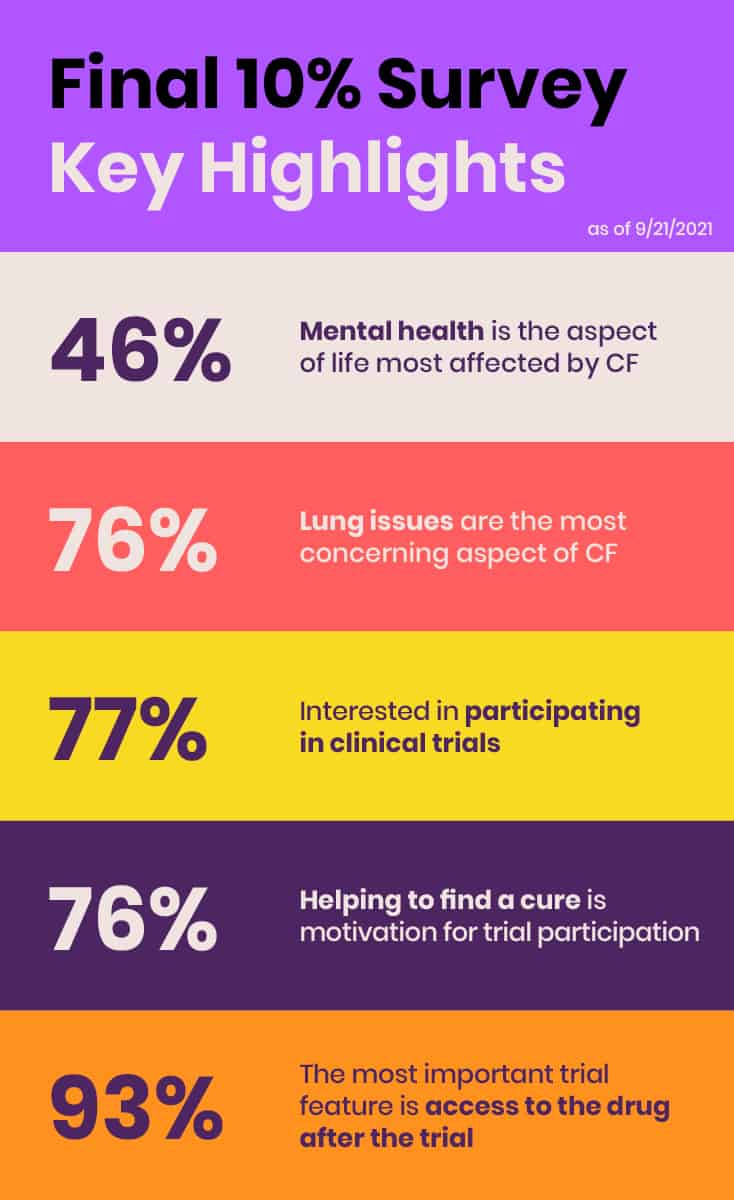
O inquérito é outro exemplo de como a EE está a identificar necessidades e a preencher lacunas críticas. Embora o inquérito se destinasse inicialmente a complementar as histórias dos seis membros da comunidade de FC na Sessão de Escuta da FDA com alguns dados quantitativos básicos, rapidamente se tornou claro que o seu valor era muito maior e mais expansivo. O inquérito produziu uma resposta robusta, com 431 inquiridos de 29 países dos cinco continentes. A EE planeou publicar os resultados num jornal com revisão por pares para garantir que estes dados estão totalmente disponíveis para o público.


