
- Lar
- A história de Emily
- Sobre nós
- Pesquisar
- Eventos
- Imprensa e Mídia
- Tome uma atitude
- Blogue
- Contato
- Doar

Advocacia
Destacando as necessidades do 10% final
A defesa e a representação dos 10% finais da comunidade de FC é uma parte essencial da missão da EE. Embora a EE tenha conquistado uma merecida reputação ao longo dos anos pela defesa eficaz da pesquisa e do desenvolvimento terapêutico para os 10% finais da comunidade de FC, houve uma percepção crescente de seu valor exclusivo no espaço regulatório - e especificamente com os principais reguladores, como a Food & Drug Administration (FDA).
Em 2021, a EE levou sua defesa à FDA por meio de Organizar uma sessão de escuta de pacientes da FDA. Esse foi um passo importante para a organização. A abordagem da EE em relação à defesa de direitos sempre colocou o paciente no banco do motorista, trabalhando lado a lado com a comunidade científica. A parceria com a FDA em uma sessão que se concentrou especificamente nas necessidades não atendidas do 10% final da comunidade de FC refletiu a voz influente e em expansão da EE em várias áreas fundamentais para o desenvolvimento terapêutico, incluindo o espaço regulatório.

As sessões de escuta de pacientes da FDA são reuniões pequenas e informais, fechadas ao público, em que grupos de defesa de pacientes falam com a equipe da FDA sobre sua experiência de viver e gerenciar uma doença. Os objetivos da sessão de escuta da EE foram compartilhar e humanizar as necessidades terapêuticas urgentes e não atendidas que permanecem para o 10% final da comunidade de FC; construir um relacionamento sólido com a FDA para incentivar a priorização e acelerar as revisões e aprovações regulatórias no futuro; e garantir que as perspectivas da comunidade de FC sejam incluídas em todos os estágios dos processos de desenvolvimento e aprovação de medicamentos.
Na reunião, a EE instruiu a equipe da FDA sobre a EE, a FC e os 10% restantes da comunidade de FC que não se beneficiam dos moduladores de CFTR atualmente disponíveis, incluindo aqueles com mutações sem sentido da FC. O evento incluiu comentários de um médico e de seis membros da comunidade de FC, incluindo indivíduos com FC, pais e irmãos de indivíduos com FC e um pai de um indivíduo falecido com FC, que compartilharam sua experiência de vida com a doença. Essas histórias profundamente pessoais e sinceras ajudaram a transmitir à FDA a urgência na busca de tratamentos para os 10% restantes da comunidade de FC.
Histórias destacadas nas sessões de escuta da FDA:
Como parte da sessão de escuta da FDA, os participantes ouviram seis membros da comunidade de FC, incluindo Abhijit Tirumala, um estudante universitário de 19 anos com fibrose cística. Como parte de seu depoimento, Abhijit contou como a FC afeta sua saúde mental e como sua vida mudaria se um novo medicamento pudesse reduzir sua dependência de tratamentos e medicamentos diários.

Em junho de 2021, a EE realizou sua primeira pesquisa global e abrangente sobre os cerca de 10% de indivíduos da comunidade de FC que não se beneficiam dos moduladores de CFTR atualmente disponíveis devido a mutações não elegíveis, efeitos colaterais ou falta de acesso. O objetivo da pesquisa "Final 10%" foi coletar informações sobre o estado de saúde, o impacto da FC, as necessidades de tratamento não atendidas e as preferências de pesquisa clínica daqueles que não se beneficiam dos moduladores de CFTR e apresentar dados e resultados preliminares na Sessão de Escuta da FDA.
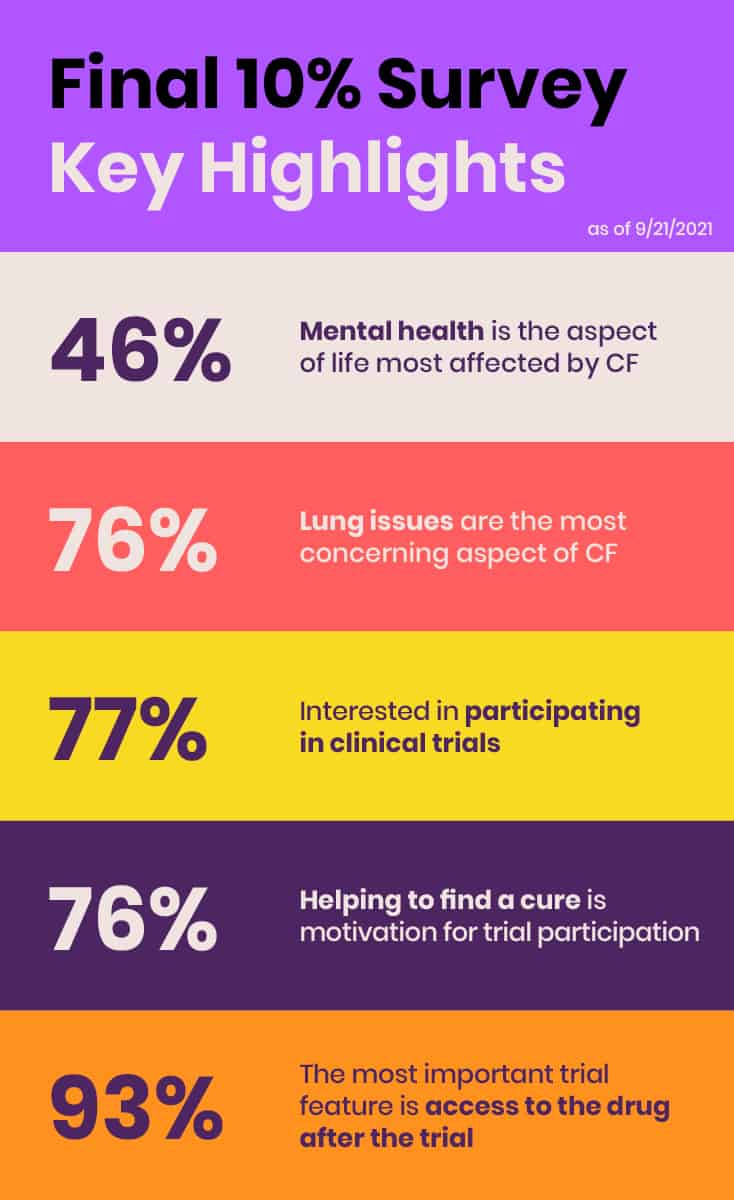
A pesquisa é outro exemplo de como a EE está identificando necessidades e preenchendo lacunas críticas. Embora a pesquisa inicialmente tivesse a intenção de complementar as histórias dos seis membros da comunidade de FC na Sessão de Escuta da FDA com alguns dados quantitativos básicos, rapidamente ficou claro que seu valor era muito maior e mais abrangente. A pesquisa gerou uma resposta robusta, com 431 respondentes de 29 países em cinco continentes. A EE planejou publicar os resultados em um periódico revisado por pares para garantir que esses dados estejam totalmente disponíveis para o público.


